Cardiomiopatia Arritmogênica do Ventrículo Direito no ECG
A cardiomiopatia arritmogênica do ventrículo direito (CAVD), também chamada displasia arritmogênica do ventrículo direito, é uma doença do músculo cardíaco que se caracteriza clinicamente por arritmias ventriculares com risco de vida e patologicamente caracterizada por distrofia progressiva do miocárdio ventricular sendo substituída por tecido fibroso ou fibroadiposo 1 2 3.
A CAVD é uma doença hereditária que pode levar à disfunção biventricular, arritmias ventriculares e morte cardíaca súbita. É uma das principais causas de morte súbita em jovens e atletas 1 2.
Epidemiologia da CAVD
A prevalência estimada de cardiomiopatia arritmogênica do ventrículo direito na população geral varia de 1:2000 a 1:5000, afectando mais frequentemente os homens do que as mulheres (até 3:1) 2 3.
A CAVD é relatada como causa de morte cardíaca súbita em 11% a 27% dos casos em doentespacientes com menos de 35 anos 4.
Apresentação clínica da cardiomiopatia arritmogênica do ventrículo direito
A fase inicial é uma fase pré-clínica conhecida como "doença oculta", que se caracteriza por uma alteração estrutural mínima ou nenhuma, com ou sem pequenas arritmias ventriculares 2 5.
É típico que a cardiomiopatia arritmogênica do ventrículo direito manifesta-se clinicamente entre a segunda e terceira década de vida 2 3. Mais raramente, os sintomas e sinais podem aparecer antes da puberdade ou na terceira idade 3.
A apresentação clínica mais frequente consiste em arritmias ventriculares e eventos ou sintomas relacionados, tais como palpitações, episódios sincopais (que ocorrem principalmente durante o exercício físico) e paragens cardíacas 5.
A morte súbita cardíaca pode ser a primeira manifestação da doença, especialmente em jovens e em atletas de competição que não diagnosticados previamente de cardiomiopatia arritmogênica do ventrículo direito 2 5.
A CAVD pode por vezes simular miocardite aguda, com dores no peito, elevação transitória do segmento ST, e alterações da onda T. Além disso, podem ser detectados valores elevados de biomarcadores cardíacos.
Os doentes com doença prolongada podem desenvolver disfunção ventricular direita ou disfunção biventricular 2 6.
Diagnóstico da cardiomiopatia arritmogênica do ventrículo direito
Actualmente, não existem testes gold-standard ou critérios patognomónicos para se fazer um diagnóstico definitivo da CAVD 1 3.
Os critérios de diagnóstico, inicialmente estabelecidos em 1994 7, foram revistos em 2010 para melhorar a sensibilidade diagnóstica, mas com o importante pré-requisito de manter a especificidade diagnóstica 3.
Os critérios da Task Force em 2010 8 favorecem o diagnóstico com ênfase nos critérios maior (cada critério maior pontua 2 pontos) e menor (cada critério menor pontua 1 ponto), que incluem 6 áreas 1 4 8:
- Alterações estruturais
- Achados histopatológicos
- Alterações da repolarização
- Alterações da despolarização
- Arritmias
- Antecedentes familiares
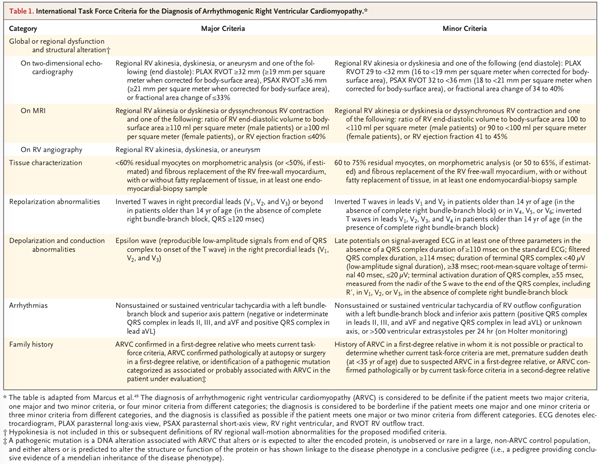
Critérios de cardiomiopatia arritmogênica do ventrículo direito, extraído de Corrado D, Link MS, et al. Arrhythmogenic Right Ventricular Cardiomyopathy 2.
Cada critério concede 2 pontos, cada critério menor concede 1 ponto, são necessários 4 pontos para realizar o diagnóstico da CAVD e uma das seguintes combinações: 2 critérios maiores, 1 critério maior e 2 critérios menores, ou 4 critérios menores 1 8.
O diagnóstico é limite se forem alcançados 3 pontos (1 critério maior e 1 critério menor, ou 3 critérios menores) 1 8.
O diagnóstico é possível se houver 2 pontos (1 critério maior ou 2 critérios menores) 1 8.
Embora estes critérios sejam mais sensíveis, há dificuldade em aplicá-los vigorosamente quando são usados para rastrear familiares ou em portadores de variantes assintomáticas, e em excluir outros diagnósticos possíveis, tais como miocardite, sarcoidose, cardiomiopatia dilatada, síndrome de Brugada, anomalia de Uhl, anomalia de Ebstein, um shunt da esquerda para a direita e hipertensão pulmonar 1.
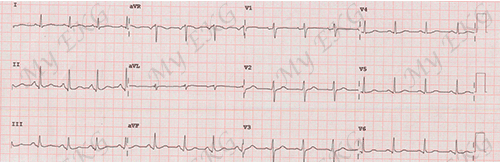
Achados electrocardiográficos na cardiomiopatia arritmogênica do ventrículo direito
O electrocardiograma tem um papel fundamental no diagnóstico da CAVD 4.
Alterações da repolarização
As alterações da repolarização são um marcador precoce e sensível da expressão da doença na CAVD 8. Uma das principais características da CAVD é a presença de ondas T invertidas nas derivações precordiais direitas em pacientes com mais de 14 anos de idade, na ausência de bloqueio do ramo direito 4 8.
A inversão das ondas T nas derivações V1, V2, V3 e em outras derivações precordiais em indivíduos saudáveis com mais de 14 anos de idade é observada em apenas 4% das mulheres saudáveis e 1% dos homens saudáveis. É portanto, um achado específico e é considerado uma alteração diagnóstica maior na CAVD 8.
O envolvimento do ventrículo esquerdo pode aparecer e pode mesmo ser a principal alteração na CAVD. As ondas T negativas podem estender-se até às derivações precordiais laterais (V4, V5 ou V6) sugerindo envolvimento ventricular esquerdo 4 5.
Alterações da despolarização
As alterações de despolarização incluem o bloqueio incompleto do ramo direito (raramente bloqueio completo), prolongamento da duração do complexo QRS em derivações precordiais com um atraso na parte ascendente da onda S 5.
Onda épsilon
Artigo relacionado: Onda epsilon.
A onda epsilon é um potencial de pequena amplitude que aparece no fim do complexo QRS e no início do segmento ST, o qual é detectado nas derivações precordiais direitas 4.
Considera-se que as ondas epsilon na CAVD representam áreas de activação retardada no ventrículo direito como resultado da substituição do tecido fibroso ou fibroadiposo do miocárdio ventricular direito, por esta razão as ondas epsilon são consideradas um critério maior 4.
As ondas epsilon são registadas em doentes com doença avançada 5.
Mais informação em: Onda epsilon.
Arritmias
As arritmias ventriculares variam de extrassístoles ventriculares frequentes a taquicardias ventriculares, que podem degenerar em fibrilação ventricular. Estas arritmias são desencadeadas ou agravadas pela estimulação adrenérgica 2.
A presença de mais de 500 extrassístoles ventriculares em 24 horas é um critério menor para o diagnóstico de cardiomiopatia arritmogênica do ventrículo direito 1 4 7.
As taquicardias ventriculares sustentadas ou não sustentadas com bloqueio do ramo esquerdo e eixo superior (complexos QRS negativos ou indeterminados nas derivações inferiores e positivos em aVL) são considerados um critério maior. Os outros padrões de taquicardia ventricular são considerados um critério menor 1 4 7.
As arritmias ventriculares sustentadas podem ocorrer em aproximadamente 70% dos pacientes 6.
Critérios eletrocardiográficos da cardiomiopatia arritmogênica do ventrículo direito
Alterações da repolarização
Maior
- Ondas T negativas nas derivações precordiais direitas (V1, V2 e V3) ou ou mais em indivíduos >14 anos de idade (na ausência de bloqueio completo do ramo direito com QRS ≥120 ms).
Menor
- Ondas T negativas nas derivações V1 e V2 em indivíduos com >14 anos de idade (na ausência de bloqueio completo do ramo direito) ou em V4, V5 ou V6.
- Ondas T negativas nas derivações V1, V2, V3 e V4 em indivíduos com >14 anos de idade na presença de bloqueio completo do ramo direito.
Alterações da despolarização/condução
Maior
- Onda epsilon (sinal de pequena amplitude reprodutível entre o fim do complexo QRS e o início da onda T) nas derivações precordiais direitas (de V1 a V3).
Menor
- Potenciais tardios, por meio de um ECG com média de sinal em 1 ou mais de 3 parâmetros, na ausência de uma duração do QRS ≥110 ms no ECG padrão:
- Duração do QRS filtrado ≥114 ms.
- Duração do sinal de baixa amplitude (<40 μV) do QRS terminal ≥38 ms.
- Raiz da média quadrada de 40 ms das voltagens dos 40 ms terminais ≤20 μV.
- Duração da activação terminal do complexo QRS ≥55 ms, medida desde o nadir da onda S até ao fim do complexo QRS, incluindo R', nas derivações V1, V2 ou V3, na ausência de bloqueio completo do ramo direito.
Arritmias
Maior
- Taquicardias ventriculares não sustentadas ou sustentadas de morfologia de bloqueio do ramo esquerdo com eixo superior (QRS negativo ou indeterminado nas derivações D2, D3 e aVF, e positivo no lead aVL).
Menor
- Taquicardias ventriculares não sustentadas ou sustentadas de TSVD, com morfologia de bloqueio do ramo esquerdo com eixo inferior (QRS positivo nas derivações D2, D3 e aVF, e negativo no lead aVL) ou eixo desconhecido, ou mais de 500 extrassístoles ventriculares por 24 horas (em monitorização de holter ECG).
Tratamento da CAVD
Os objectivos mais importantes na gestão clínica dos pacientes com cardiomiopatia arritmogênica do ventrículo direito incluem 3:
- Redução da mortalidade por morte súbita ou insuficiência cardíaca
- Prevenção da progressão da doença que leva à disfunção do ventrículo direito, ventrículo esquerdo ou biventricular.
- Atenuação dos sintomas e melhoria da qualidade de vida, reduzindo palpitações, recorrência das taquicardias ventriculares e choques do CDI.
As opções terapêuticas incluem mudanças de estilo de vida, tratamento medicamentoso, ablação por cateter, implante de CDI e transplante cardíaco.
As Directrizes 2017 AHA/ACC/HRS para a gestão do paciente com arritmias ventriculares e a prevenção da morte cardíaca súbita 9 e o International Task Force Consensus Statement de 2015 para o tratamento da cardiomiopatia arritmogênica do ventrículo direito/displasia arritmogênica do ventrículo direito 10 recomendam:
Mudanças no estilo de vida
Os pacientes com cardiomiopatia arritmogênica do ventrículo direito têm um risco aumentado de morte súbita durante o esforço 9 10. Os doentes com um diagnóstico definitivo de CAVD não devem participar em desportos competitivos ou de resistência e devem evitar exercícios intensos.
Tratamento farmacológico
Os beta-bloqueadores são recomendados em pacientes com CAVD com arritmias ventriculares para prevenir arritmias ventriculares induzidas pelo stress, e para a gestão da insuficiência cardíaca 9 10.
Os beta-bloqueadores podem ser úteis em pacientes assintomáticos com CAVD sem arritmias ventriculares ou disfunções ventriculares 9.
Cardioversor desfibrilador implantável
A implantação de um cardioversor desfibrilador implantável (CDI) também é recomendada em pacientes com elevado risco de morte cardíaca súbita (reanimados por paragem cardíaca súbita, taquicardia ventricular sustentada, disfunção ventricular grave com FEVE ou FEVD ≤35%) 9 10.
A implantação de um CDI também deve ser considerada em pacientes com CAVD e síncope inexplicada, taquicardia ventricular não sustentada, ou disfunção ventricular direita ou esquerda moderada 9 10.
Ablação por cateter
Ablação por cateter da taquicardia ventricular pode ser benéfica em doentes com CAVC e taquicardias ventriculares sintomáticas e recorrente em que um beta-bloqueador é ineficaz ou não tolerado 9 10.
Transplante cardíaco
Os doentes com CAVD e insuficiência cardíaca intratável ou taquiarritmias ventriculares descontroladas podem necessitar de um transplante cardíaco 10.
O transplante cardíaco é recomendado como a opção terapêutica final em pacientes com CAVD com insuficiência cardíaca não responsiva ou episódios recorrentes de taquicardia/fibrilação ventricular refratária à ablação por cateter em centros experientes ou terapia de CDI 10.
Referências
- 1. Chahal A, Nosheen Reza N, Santangeli P. Risk Stratification in Arrhythmogenic RV Cardiomyopathy/Dysplasia Without an ICD. Expert Analysis. [Internet]. The American College of Cardiology; Feb 26, 2019 [cited: October 25, 2019]. Available on: https://www.acc.org/latest-in-cardiology/...
- 2. Corrado D, Link MS, Calkins H. Arrhythmogenic Right Ventricular Cardiomyopathy. N Engl J Med 2017; 376:61-72. doi: 10.1056/NEJMra1509267.
- 3. Pilichou K, Thiene G, Bauce B, et al. Arrhythmogenic cardiomyopathy. Orphanet J Rare Dis. 2016;11:33. doi: 10.1186/s13023-016-0407-1.
- 4. Quarta G, Elliott PM. Diagnostic Criteria for Arrhythmogenic Right Ventricular Cardiomyopathy. Rev Esp Cardiol. 2012; 65(7), 599–605. doi: 10.1016/j.rec.2012.02.015.
- 5. Corrado D, Basso C, Judge DP. Arrhythmogenic Cardiomyopathy. Circulation Research. 2017;121:784–802. doi: 10.1161/CIRCRESAHA.117.309345
- 6. Groeneweg JA, Bhonsale A, James CA et al. Clinical Presentation, Long-Term Follow-Up, and Outcomes of 1001 Arrhythmogenic Right Ventricular Dysplasia/Cardiomyopathy Patients and Family Members. Circulation: Cardiovascular Genetics. 2015;8:437–446. doi: 10.1161/CIRCGENETICS.114.001003.
- 7. McKenna WJ, Thiene G, Nava A, Fontaliran F, et al. Diagnosis of arrhythmogenic right ventricular dysplasia/cardiomyopathy. Task Force of the Working Group Myocardial and Pericardial Disease of the European Society of Cardiology and of the Scientific Council on Cardiomyopathies of the International Society and Federation of Cardiology. Br Heart J. 1994;71:215-218. doi: 10.1136/hrt.71.3.215.
- 8. Marcus FI1, McKenna WJ, Sherrill D, et al. Diagnosis of arrhythmogenic right ventricular cardiomyopathy/dysplasia: proposed modification of the Task Force Criteria. Eur Heart J. 2010 Apr;31(7):806-14. doi: 10.1093/eurheartj/ehq025.
- 9. Al-Khatib SM, Stevenson WG, Ackerman MJ, et al. 2017 AHA/ACC/HRS Guideline for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death. A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. Circulation. 2018;138:e272–e391. doi: 10.1161/CIR.0000000000000549.
- 10. Corrado D, Wichter T, Link MS, et al. Treatment of Arrhythmogenic Right Ventricular Cardiomyopathy/Dysplasia. An International Task Force Consensus Statement. Circulation. 2015;132:441–453. doi: 10.1161/CIRCULATIONAHA.115.017944
Se você gostou... Compartilhe.